NAD+水平随着年龄的增长而下降,这与衰老和年龄相关的多种疾病有关。然而,支持NAD+的前体物可补充这一关键分子,从而恢复其正常水平,以焕发青春之活力。
目录
4.1.NMN
4.2.烟酰胺核糖
4.3.烟酰胺
4.4.烟酸
4.5.色氨酸
6.参考文献
NAD+(烟酰胺腺嘌呤二核苷酸)随着年龄的增长而减少,导致细胞能量产生下降并促进炎症产生。这些因素会加速衰老,并增加与年龄相关的慢性疾病的发病率1。事实上,在整个衰老过程中以及在许多与年龄相关的疾病中,研究人员观察到NAD+的可用性降低2。
NAD+分子在细胞代谢中起着核心作用。它还在DNA修复、细胞动力(线粒体)的产生及其能量生产能力中发挥关键作用。此外,由于其免疫再生特性,NAD+也有助于缓解炎症3。随着NAD+水平与年龄的增长而减少,细胞功能的这些方面也会下降。
使用动物模型的科学研究表明,在衰老过程中增加NAD+水平可以在一定程度上延缓衰老、延长寿命,甚至在一定程度上逆转衰老4。据此,提高NAD+水平对不同年龄相关的疾病和病症有积极影响,包括胰岛素不敏感、2型糖尿病、心血管疾病、神经退行性变和癌症5。
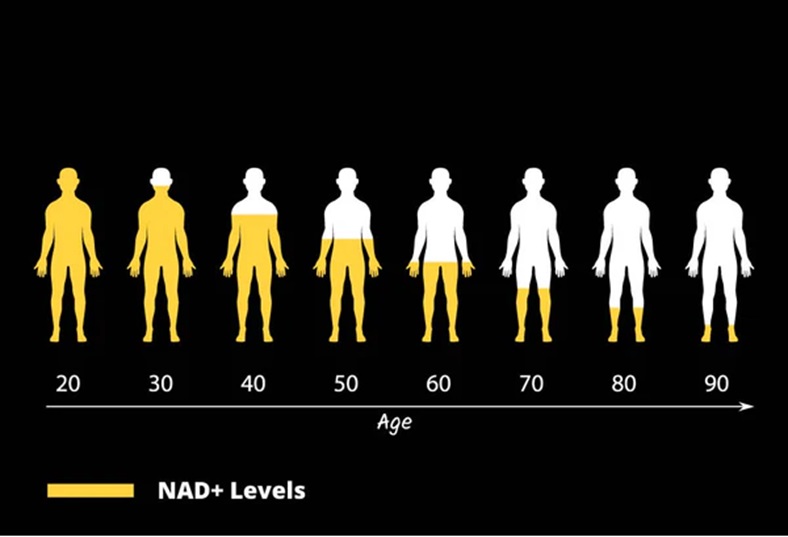
图1,NAD+水平随着年龄增长而下降(来源:互联网)
1906年,英国生物化学家Arthur Harden和William John Young发现了NAD+6。通过对酒精发酵过程中酵母提取物的研究,他们分离出NAD+。经过漫长而艰难的过程,Hans-von-Euler-Chelpin纯化了NAD+7。30年后的1936年,德国科学家、诺贝尔奖获得者Otto Heinrich Warburg在细胞能量产生位点发现了NAD+辅酶的电子交换功能8。
1938年,Conrad Elvehjem鉴定了NAD+的维生素前体,他表明肝脏中的烟酰胺具有“抗黑舌作用”9。1939年,Elvehjem提供了烟酸可用于合成NAD+的证据。20世纪40年代初,Arthur Kornberg在NAD+的生物合成途径中发现了一种酶—烟酰胺单核苷酸腺苷酸转移酶(NMNAT)10。1949年,美国生物化学家Morris Friedkin和Albert L.Lehninger证明,添加氢(NADH)的NAD+将柠檬酸循环等代谢途径与三磷酸腺苷(ATP)分子形式的细胞能量合成联系起来11。1958年,Jack Preiss和Philip Handler发现了参与NAD+生物合成途径的中间前体分子和酶。因此,从烟酸中回收合成NAD+被称为Preiss-Handler途径11。
NAD+与新陈代谢和健康衰老的关系在21世纪仍然是一个密切的研究领域12。2000年,Shin Ichiro Imai及其同事在Leonard P. Guarente实验室发现了Sirtuins,这是一种功能依赖于NAD+的蛋白质,参与DNA修复和细胞抗氧化活性13,这引起了人们对NAD+的高度兴趣。根据这些思路,Imai在2009年提出了“NAD+世界假说”,该假说认为Sirtuin1和NAD+合成酶烟酰胺磷酰转移酶(NAMPT)调节哺乳动物的衰老和寿命14。2016年,Imai将他的假说扩展到“NAD+世界假说2.0”,假设脂肪组织细胞外的NAMPT(细胞外NAMPT)维持大脑激素控制中心下丘脑的NAD+,以保护骨骼肌健康,防止衰老过程中的虚弱15。
色氨酸、烟酸、烟酰胺、烟酰胺核糖(NR)和烟酰胺单核苷酸(NMN)是哺乳动物NAD+的前体。细胞可以通过三种途径产生NAD+并在人体内重复使用:色氨酸的从头合成途径,烟酸或烟酸核糖的Preiss-Handler途径,以及烟酰胺、NR和NMN的补救途径16。
由于NAD+主要通过烟酰胺(维生素B3的一种)、NR和NMN的NAD+补救途径产生,这些补救途径分子最有可能成为NAD+增强剂,其中,NMN仅需要一个步骤即可转化为NAD+16。烟酸和色氨酸则需要更多的步骤才能产生NAD+,从而降低这两种分子的吸引力(如图2)。
鉴于NAD+水平随着年龄的增长而下降,目前正在对其药理性恢复进行深入研究。沿着这些路线,NAD+替代的方法包括NAD+前体,如NR、NMN和烟酸补充。
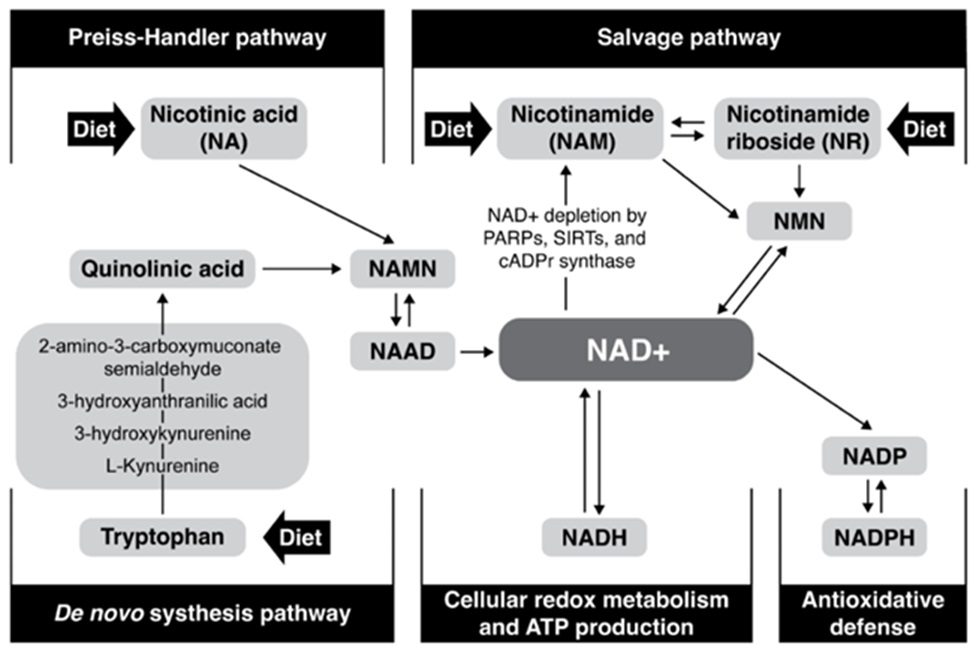
图2,NAD+的生物合成途径(Poljsak et al., 2022)
3.1.烟酰胺单核苷酸(NMN)
NMN对啮齿类动物具有广泛的长寿益处。这些益处包括帮助对抗心血管、代谢和神经系统与年龄相关的疾病。
尽管迄今为止没有研究直接表明NMN可以延长啮齿动物的寿命,但许多研究表明,NMN可以促进无病寿命(健康寿命)。例如,Shin Ichiro Imai实验室的一项研究表明,在衰老小鼠的水中补充NMN可以抑制与年龄相关的体重增加,增强能量代谢,促进体力活动,增加胰岛素敏感性,改善眼视力功能17。
至于NMN对年龄相关疾病的作用,该分子已在心血管疾病的小鼠研究中显示出前景。例如,NMN已被证明可以缓解随着年龄增长而出现的常见心脏病,即心脏瘢痕(纤维化)。该项研究表明,NMN可以预防心脏增大和纤维化,从而预防心脏病18。另一项针对小鼠的心血管研究表明,NMN可以防止血管细胞进入非增殖状态,在这种状态下,它们会释放出称为衰老的炎症分子19。NMN还使小鼠的血压恢复正常,这可能是通过改善血管健康和减少衰老血管细胞的数量来实现的19。这些研究表明,NMN可能有助于在衰老过程中保持心脏功能。
啮齿动物研究还表明,NMN可以改善衰老过程中的新陈代谢20。对于小鼠脂肪细胞,研究人员已经表明NMN可以增加代谢活性并减少炎症。如果这些发现可以转化为人类,它们表明NMN可以促进减肥和健康的能量代谢。
神经系统疾病,如记忆力丧失,会随着年龄的增长而发生。对一些人来说,这些疾病会引发全面的神经退行性病变。一些啮齿动物研究表明,NMN可用于阻止或减缓与年龄相关的神经退行性疾病。据此,一项小鼠研究表明,NMN可以恢复糖尿病诱导的记忆障碍小鼠的记忆能力21。在这项研究中,NMN保存了糖尿病患者因营养缺乏而死亡的神经元。其他研究表明,NMN可以改善脑血管生成,增加脑血流量和功能22。这些研究支持NMN有助于保持认知,并对抗与年龄相关的神经系统疾病。
3.2.烟酰胺核糖(NR)
在啮齿类动物研究中,NR也被证明可以提高健康寿命。根据这些原理,一项NR小鼠研究表明,补充该分子可以提高老年小鼠的跑步耐力4。这些身体功能的改善是由增强的线粒体健康引起的,NR诱导的线粒体耗氧量增加证明了这一点。同一项研究还表明,NR可使小鼠的平均寿命延长约5%。这些发现使NR补充剂有望促进更健康的衰老。
4.1.烟酰胺单核苷酸(NMN)
NMN是最直接的NAD+前体,离形成NAD+仅需一步酶促作用。相对于其他前体,NMN最近才在治疗年龄相关缺陷的临床试验中进行测试。一项针对男性的研究表明,NMN能有效提高血液NAD+水平23。研究表明,仅需服用125mg NMN四周就使血液NAD+水平几乎翻了一番,从而使NAD+水平趋于平稳24。另一项针对MIB-626(David Sinclair所创公司拥有)NMN的研究也使血液NAD+水平翻了一番,特别是在中老年人中25。
几项研究表明,NMN可以改善身体表现和睡眠质量。在老年人中,NMN可以改善睡眠质量和身体表现26。这种剂量(250mg)的NMN除了增强肌肉功能和灵活性外,还提高了老年男性的握力和行走速度27。其他研究也表明NMN可以改善身体表现28和睡眠质量29。此外,NMN改善了业余跑步者的肌肉氧利用率和运动表现30。
在糖尿病前期、超重或肥胖的绝经后妇女中,NMN增加了肌肉和白细胞NAD+水平,并改善了胰岛素敏感性,这表明NMN可以预防2型糖尿病31。同样在绝经后妇女中,NMN改善了葡萄糖和胆固醇代谢、激素水平以及备受关注的皮肤衰老标志物32。
NMN补充也被证明可以增加老年人白细胞的端粒长度。端粒的缩短与衰老有关,因此这些发现表明NMN逆转了分子衰老的各个方面33。为了支持这一点,NMN已被证明可以降低老年人白细胞的生物学年龄34。
总体而言,NMN似乎可以改善老年人的身体表现和睡眠质量,并改善皮肤老化和胰岛素敏感性。
4.2.烟酰胺核糖(NR)
与NMN一样,NR是人类中研究得更深入的NAD+前体之一。NR已在牛奶中找到,可以作为一种膳食补充剂。
临床研究表明,NR可分别提高中老年人全血35和白细胞36NAD+水平。然而,即使在高剂量下37,它也不会增加老年人肌肉中的NAD+38。
尽管NR似乎不会增加肌肉NAD+水平,但它会减少血液和心脏炎症标志物39。这些发现表明NR可以减少炎症,而炎症是慢性激活时导致衰老的主要因素。
至于耐力运动,NR似乎只对老年人有益。年轻男性补充NR一周后,运动耐力没有改善40。然而,NR确实改善了老年人的运动表现41,但没有改善年轻人的运动成绩。
在肥胖的老年男性中,NR并没有改善胰岛素敏感性或身体成分42。然而,在一项规模小得多的研究中,NR改善了超重或肥胖成年人的身体成分43。尽管如此,在另一项针对超重或肥胖的中老年人的研究中,NR除了增加血液NAD+水平外,没有太多影响44。因此,NR对中老年人身体成分的影响尚不清楚。
一些公司已经将天然NR与一种植物来源的抗氧化剂紫檀芪结合在一起。这种组合已被证明可以提高老年人的血液NAD+水平,降低舒张压,并改善身体表现45。这种组合还可以减少患有非酒精性脂肪肝病(NAFLD,即脂肪肝)的成年人的炎症46。此外,NR和紫檀芪的组合似乎可以减缓运动神经元病(ALS,肌萎缩侧索硬化症)的进展47。
如ALS所示,NR在神经退行性疾病方面有着更为广阔的前景。当与抗氧化代谢促进化合物相结合时,NR已被证明可以改善阿尔茨海默症患者的认知和大脑结构48。此外,单独使用NR可以改善帕金森病的潜在缺陷49。总的来说,NR,尤其是与抗氧化剂结合时,似乎可以预防神经退行性变并改善认知。
4.3.烟酰胺
烟酰胺存在于各种肉类、豆类和坚果中。烟酰胺已在两项人体试验中用于预防1型糖尿病,一项在2004年,另一项在2006年50。在这两项试验中,烟酰胺都未能预防1型糖尿病。还需要更多的研究来发现烟酰胺单独是否有潜力对抗人类衰老。尽管如此,烟酰胺与D-核糖结合已被证明可以改善中年人的胰岛素敏感性和降低皮质醇水平51。
4.4.烟酸
烟酸可以在牛肉、鱼和家禽等食物中找到。在一项人体试验中,患有线粒体肌病的神经肌肉疾病的患者服用1000mg烟酸后,血液和肌肉NAD+水平得到补充,力量和表现也得到改善52。
烟酸被用于降低胆固醇53,但会引起潮红,导致使用烟酸衍生物—阿西莫司(Acipimox)。阿西莫司已被证明能增强2型糖尿病患者肌肉的能量产生和线粒体功能54。由于这些糖尿病患者的平均年龄约为58岁,烟酸及其衍生物可能是患有2型糖尿病的老年人的好选择。
4.5.色氨酸
色氨酸是一种氨基酸,存在于牛奶、鸡肉和坚果等富含蛋白质的食物中。它可能是最差的NAD+前体55,因为它需要更多的生物合成步骤才能成为NAD+。因此,34至86mg色氨酸的膳食摄入量相当于1mg尼克酸(烟酸)56,57。
(色氨酸化学结构)
根据人体研究,似乎大多数NAD+前体是安全的,对大多数人来说几乎没有副作用(除了未修饰的烟酸可导致潮红)。此外,每种前体都经过了不同年龄相关缺陷的测试,因此尚不清楚哪种前体更适合某些缺陷。
了解更多有关NMN或NR内容、机制和作用、产品成分和品牌以及购买路径等,可参阅本网专文:
来源:本网编辑2024.04.26.首版
1. McReynolds MR et al. Age-related NAD+
decline. Exp Gerontol. 2020 Feb 22:134:110888.
2. Katsyuba E et al. NAD+ homeostasis in
health and disease. Nat Metab. 2020 Jan;2(1):9-31.
3. Covarrubias AJ et al. NAD+ metabolism
and its roles in cellular processes during ageing. Nat Rev Mol Cell Biol. 2021
Feb;22(2):119-141.
4. Zhang H et al. NAD⁺ repletion improves mitochondrial and stem cell function and
enhances life span in mice. Science. 2016 Jun 17;352(6292):1436-43.
5. Helman T et al. Importance of NAD+
Anabolism in Metabolic, Cardiovascular and Neurodegenerative Disorders. Drugs
Aging. 2023 Jan;40(1):33-48.
6. Xie N et al. NAD+ metabolism:
pathophysiologic mechanisms and therapeutic potential. Signal Transduct Target
Ther. 2020 Oct 7;5(1):227.
7. Nicotinamide adenine dinucleotide at. https://en.wikipedia.org/wiki/Nicotinamide_adenine_dinucleotide
8. Palmer RD et al. Precursor comparisons
for the upregulation of nicotinamide adenine dinucleotide. Novel approaches for
better aging. Aging Med (Milton). 2021 Sep; 4(3): 214–220.
9. Braidy N et al. Role of Nicotinamide
Adenine Dinucleotide and Related Precursors as Therapeutic Targets for
Age-Related Degenerative Diseases: Rationale, Biochemistry, Pharmacokinetics,
and Outcomes. Antioxid Redox Signal. 2019 Jan 10; 30(2): 251–294.
10. Jayaram HN et al. NMNAT expression and
its relation to NAD metabolism. Curr Med Chem. 2011;18(13):1962-72.
11. Zapata‐Pérez R et al. NAD+ homeostasis
in human health and disease. EMBO Mol Med. 2021 Jul 7; 13(7): e13943.
12. Imai S-I and Guarente L. NAD+ and
sirtuins in aging and disease. Trends Cell Biol. 2014 Aug;24(8):464-71.
13. Imai S-I and Guarente L. 10 Years of
NAD-Dependent SIR2 Family Deacetylases–Implications for Metabolic Diseases. Trends Pharmacol Sci. 2010 May; 31(5):
212–220.
14. Imai S-I. The NAD World: a new systemic
regulatory network for metabolism and aging--Sirt1, systemic NAD biosynthesis,
and their importance. Cell Biochem Biophys. 2009;53(2):65-74.
15. Imai S-I. The NAD World 2.0: the
importance of the inter-tissue communication mediated by NAMPT/NAD+/SIRT1 in
mammalian aging and longevity control. NPJ Syst Biol Appl. 2016; 2: 16018.
16. Poljšak B et al. Current Uncertainties
and Future Challenges Regarding NAD+ Boosting Strategies. Antioxidants (Basel).
2022 Aug 24;11(9):1637.
17. Mills KF et al. Long-Term
Administration of Nicotinamide Mononucleotide Mitigates Age-Associated
Physiological Decline in Mice. Cell Metab. 2016, 24, 795–806.
18. Wu K et al. Nicotinamide mononucleotide
attenuates isoproterenol-induced cardiac fibrosis by regulating oxidative
stress and Smad3 acetylation. Life Sci. 2021 Mar 3;274:119299.
19. Gan L et al. CD38 deficiency alleviates
Ang II-induced vascular remodeling by inhibiting small extracellular
vesicle-mediated vascular smooth muscle cell senescence in mice. Signal
Transduct Target Ther. 2021 Jun 11;6(1):223.
20. Majeed Y et al. SIRT1 promotes lipid
metabolism and mitochondrial biogenesis in adipocytes and coordinates
adipogenesis by targeting key enzymatic pathways. Sci Rep. 2021 Apr
14;11(1):8177.
21. Chandrasekaran K et al. Nicotinamide
Mononucleotide Administration Prevents Experimental Diabetes-Induced Cognitive
Impairment and Loss of Hippocampal Neurons. Int J Mol Sci. 2020 May
26;21(11):3756.
22. Kiss T et al. Nicotinamide
mononucleotide (NMN) treatment attenuates oxidative stress and rescues
angiogenic capacity in aged cerebromicrovascular endothelial cells: a potential
mechanism for the prevention of vascular cognitive impairment. Geroscience.
2019 Oct;41(5):619-630.
23. Irie J et al. Effect of Oral
Administration of Nicotinamide Mononucleotide on Clinical Parameters and
Nicotinamide Metabolite Levels in Healthy Japanese Men. 2020 Feb
28;67(2):153-160.
24. Okabe K et al. Oral Administration of
Nicotinamide Mononucleotide Is Safe and Efficiently Increases Blood
Nicotinamide Adenine Dinucleotide Levels in Healthy Subjects. Front Nutr. 2022
Apr 11;9:868640.
25. Pencina K et al. MIB-626, an Oral
Formulation of a Microcrystalline Unique Polymorph of β-Nicotinamide
Mononucleotide, Increases Circulating Nicotinamide Adenine Dinucleotide and its
Metabolome in Middle-aged and Older Adults. J Gerontol A Biol Sci Med Sci. 2023
Jan 26;78(1):90-96.
26. Kim M et al. Effect of 12-Week Intake
of Nicotinamide Mononucleotide on Sleep Quality, Fatigue, and Physical
Performance in Older Japanese Adults: A Randomized, Double-Blind
Placebo-Controlled Study. Nutrients. 2022 Feb 11;14(4):755.
27. Igarashi M et al. Chronic nicotinamide
mononucleotide supplementation elevates blood nicotinamide adenine dinucleotide
levels and alters muscle function in healthy older men. NPJ Aging. 2022 May
1;8(1):5.
28. Yi L et al. The efficacy and safety of
β-nicotinamide mononucleotide (NMN) supplementation in healthy middle-aged
adults: a randomized, multicenter, double-blind, placebo-controlled,
parallel-group, dose-dependent clinical trial. Geroscience. 2023 Feb;45(1):29-43.
29. ZHAO B et al. Clinical observation of
the effect of nicotinamide mononucleotide on the improvement of insomnia in
middle-aged and old adults. American Journal of Translational Medicine.
2022;6(4),167–176.
30. Liao B et al. Nicotinamide
mononucleotide supplementation enhances aerobic capacity in amateur runners: a
randomized, double-blind study. J Int Soc Sports Nutr. 2021 Jul 8;18(1):54
31. Yoshino M et al. Nicotinamide
mononucleotide increases muscle insulin sensitivity in prediabetic women.
Science. 2021 Jun 11;372(6547):1224-1229.
32. Morita Y et al. Clinical evaluation of
changes in biomarkers by oral intake of NMN. Glycative Stress Research. 2022
Jun;9(2).33-41.
33. Niu KM et al. The Impacts of Short-Term
NMN Supplementation on Serum Metabolism, Fecal Microbiota, and Telomere Length
in Pre-Aging Phase. Front Nutr. 2021 Nov 29;8:756243.
34. Shen X et al. Scale bar of aging
trajectories for screening personal rejuvenation treatments. Comput Struct
Biotechnol J. 2022 Oct 21;20:5750-5760.
35. Airhart SE et al. An open-label,
non-randomized study of the pharmacokinetics of the nutritional supplement
nicotinamide riboside (NR) and its effects on blood NAD+ levels in healthy
volunteers. PLoS One. 2017 Dec 6;12(12):e0186459.
36. Martens CR et al. Chronic nicotinamide
riboside supplementation is well-tolerated and elevates NAD+ in healthy
middle-aged and older adults. Nat Commun. 2018 Mar 29;9(1):1286.
37. Dollerup OL et al. Nicotinamide
riboside does not alter mitochondrial respiration, content or morphology in
skeletal muscle from obese and insulin-resistant men. J Physiol. 2020
Feb;598(4):731-754.
38. Elhassan YS et al. Nicotinamide
Riboside Augments the Aged Human Skeletal Muscle NAD+ Metabolome and Induces
Transcriptomic and Anti-inflammatory Signatures. Cell Rep. 2019 Aug 13; 28(7):
1717–1728.e6.
39. Zhou B et al. Boosting NAD level
suppresses inflammatory activation of PBMCs in heart failure. J Clin Invest.
2020 Nov 2;130(11):6054-6063.
40. Stocks B et al. Nicotinamide riboside
supplementation does not alter whole-body or skeletal muscle metabolic
responses to a single bout of endurance exercise. J Physiol. 2021
Mar;599(5):1513-1531.
41. Dolopikou CF et al. Acute nicotinamide
riboside supplementation improves redox homeostasis and exercise performance in
old individuals: a double-blind cross-over study. Eur J Nutr. 2020
Mar;59(2):505-515.
42. Dollerup OL et al. A randomized
placebo-controlled clinical trial of nicotinamide riboside in obese men:
safety, insulin-sensitivity, and lipid-mobilizing effects. Am J Clin Nutr. 2018
Aug 1;108(2):343-353.
43. Remie CME et al. Nicotinamide riboside
supplementation alters body composition and skeletal muscle acetylcarnitine
concentrations in healthy obese humans. Am J Clin Nutr. 2020 Aug
1;112(2):413-426.
44. Conze D et al. Safety and Metabolism of
Long-term Administration of NIAGEN (Nicotinamide Riboside Chloride) in a
Randomized, Double-Blind, Placebo-controlled Clinical Trial of Healthy
Overweight Adults. Sci Rep. 2019 Jul 5;9(1):9772.
45. Dellinger RW et al. Repeat dose NRPT
(nicotinamide riboside and pterostilbene) increases NAD+ levels in humans
safely and sustainably: a randomized, double-blind, placebo-controlled study.
NPJ Aging Mech Dis. 2017 Nov 24:3:17.
46. Dellinger RW et al. NRPT reduces
markers of hepatic inflammation in non-alcoholic fatty liver disease: a
double-blind, placebo-controlled clinical trial. Hepatology. 2023 Sep
1;78(3):863-877.
47. de la Rubia JE et al. Efficacy and
tolerability of EH301 for amyotrophic lateral sclerosis: a randomized,
double-blind, placebo-controlled human pilot study. Amyotroph Lateral Scler
Frontotemporal Degener. 2 019 Feb;20(1-2):115-122.
48. Yulug B et al. Combined Metabolic
Activators Improves Cognitive Functions in Alzheimer’s Disease Patients: a
randomised, double-blinded, placebo-controlled phase-II trial. Transl
Neurodegener. 2023 Jan 26;12(1):4.
49. Brakedal B et al. The NADPARK study: A
randomized phase I trial of nicotinamide riboside supplementation in
Parkinson's disease. Cell Metab. 2022 Mar 1;34(3):396-407.e6.
50. Cabrera-Rode E et al. Effect of
standard nicotinamide in the prevention of type 1 diabetes in first degree
relatives of persons with type 1 diabetes. Autoimmunity. 2006 Jun;39(4):333-40.
51. Xue Y et al. A Combination of
Nicotinamide and D-Ribose (RiaGev) Is Safe and Effective to Increase NAD+
Metabolome in Healthy Middle-Aged Adults: A Randomized, Triple-Blind,
Placebo-Controlled, Cross-Over Pilot Clinical Trial. Nutrients. 2022 May 26;14(11):2219.
52. Pirinen E et al. Niacin Cures Systemic
NAD+ Deficiency and Improves Muscle Performance in Adult-Onset Mitochondrial
Myopathy. Cell Metab. 2020 Jun 2;31(6):1078-1090.e5.
53. Carlson LA. Nicotinic acid: the
broad-spectrum lipid drug. A 50th anniversary review. J Intern Med. 2005
Aug;258(2):94-114.
54. van de Weijer T et al. Evidence for a
direct effect of the NAD+ precursor acipimox on muscle mitochondrial function
in humans. Diabetes. 2015 Apr;64(4):1193-201
55. IKEDA M et al. STUDIES ON THE
BIOSYNTHESIS OF NICOTINAMIDE ADENINE DINUCLEOTIDE. II. A ROLE OF PICOLINIC
CARBOXYLASE IN THE BIOSYNTHESIS OF NICOTINAMIDE ADENINE DINUCLEOTIDE FROM
TRYPTOPHAN IN MAMMALS. J Biol Chem. 1965 Mar:240:1395-401.
56. ODS of NIH of USA. Available at. https://ods.od.nih.gov/factsheets/Niacin-HealthProfessional/
57. GOLDSMITH GA. Niacin-tryptophan
relationships in man and niacin requirement. Am J Clin Nutr. 1958
Sep-Oct;6(5):479-86.
