导言:研究发现,一种名为p38gamma的酶可以防止与记忆丧失相关的毒性。免疫细胞上的CD38在衰老过程中消耗生命必需分子NAD+及其前体NMN。
重要的化合物烟酰胺腺嘌呤二核苷酸(NAD+)与细胞中的酶结合,这些酶参与为身体产生能量的反应,以及被称为PARP和Sirtuins的酶,以维持细胞的健康。NAD+水平随着年龄的增长而下降,这会导致维持生命的化学反应(代谢)功能障碍和整体身体素质下降,但这种情况是如何发生的尚不清楚。科学家们提出了细胞中NAD+水平在衰老过程中下降的多种机制:参与NAD+合成的细胞中一种名为NAMPT的酶水平降低,DNA修复酶PARP1对NAD+的消耗增加,以及消耗NAD+的CD38酶水平增加。CD38的抑制在按时间顺序排列的衰老过程中保持了NAD+组织水平,但CD38在消耗NAD+中的作用的几个方面在衰老研究领域仍不清楚,例如哪些细胞在衰老过程中拥有CD38,是什么驱动CD38水平增加,以及CD38在调节NAD+及其前体分子水平中发挥什么作用。
根据明尼苏达州梅奥诊所(Mayo Clinic)的Chini及其同事在《自然-代谢》(Nat Metab)上发表的一项研究表明,由于衰老过程引起的炎症,CD38在免疫细胞外部的呈现随着年龄的增长而增加,CD38的积累导致NAD+及其前体分子烟酰胺单核苷酸(NMN)水平下降。
来自免疫细胞表面的CD38酶降低NAD+水平的证据来自科学家在小鼠之间转移骨髓的实验。没有CD38酶的转基因小鼠接受了正常小鼠的骨髓,因为正常小鼠的骨髓含有可以恢复具有CD38酶细胞存在的干细胞。在通常含有高水平免疫细胞的组织中,如肠和脾,在没有CD38的小鼠中,随着CD38活性的增加,NAD+水平下降,而CD38活性通过骨髓移植恢复,这表明CD38降低了NAD+水平。
研究结果还表明,炎症诱导免疫细胞聚集CD38,导致NAD+和NMN水平下降。用一种叫做脂多糖的炎症诱导分子治疗被称为白色脂肪组织(WAT)的脂肪组织导致NAD+和NMN水平降低。科学家再次将正常小鼠的骨髓移植到没有CD38的小鼠身上的实验表明,脂多糖引起的炎症加剧了CD38降低NAD+和NMN水平的作用。这表明炎症可以增加CD38对NAD+和NMN的消耗。
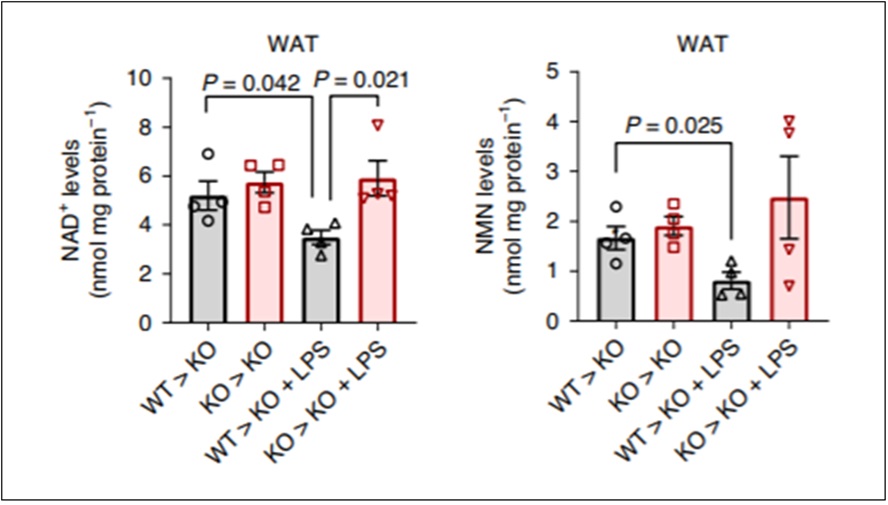
图示. 将骨髓从正常(WT)小鼠转移到没有CD38 (KO)的小鼠身上,导致NAD+和NMN水平显著降低,炎症加剧了这些降低。左图显示,与从没有CD38的小鼠到没有CD38的小鼠(KO > KO)的骨髓移植相比,从没有CD38的小鼠到没有CD38的小鼠(KO > KO)的骨髓移植降低了NAD+水平。脂多糖(LPS)的添加,引起炎症,加剧了对NAD+水平的影响。右图显示了相同的实验对NMN水平的影响。
该研究继续证明,呈递CD38的免疫细胞在过度衰老的组织中积累,这些细胞分泌与衰老组织相关的可溶性因子。此外,CD38的积累可以用这些与衰老过程相关的可溶性因子诱导。研究人员从显示出衰老迹象的老年细胞中提取了一种溶液,并将其添加到白色脂肪组织中,从而导致组织NAD+下降。该数据表明,与衰老细胞相关的可溶性因子导致NAD+水平降低。
更重要的是,研究人员证明CD38酶活性存在于免疫细胞表面,这些细胞分泌分子来刺激M1巨噬细胞的免疫反应,这些巨噬细胞上的CD38酶调节NAD+前体NMN的可用性。科学家们用脂多糖诱导M1巨噬细胞炎症,然后用NMN处理。他们观察到,在脂多糖处理后,含有巨噬细胞的溶液中NMN水平下降,但这种作用被CD38抑制剂Ab68逆转。这些结果表明炎症促进了M1巨噬细胞通过CD38消耗NMN。
“我们研究的一个关键发现是,NMN是CD38的主要底物之一,”科学家们在他们的出版物中提到CD38对NMN的消耗时说道。他们接着说,CD38的NMN消耗活性通过控制NMN的可用性来调节NAD+水平。
按照CD38作为NMN耗竭来源的思路,科学家们发现给老年小鼠服用CD38抑制剂Ab68可以促进NMN的NAD+增强作用。与年轻小鼠相比,这些NAD+增强作用在老年小鼠中显著增加,这是由于细胞NAD+水平随着年龄的增长而自然降低。用于收集该数据的实验比较了在3个月大(年轻)和18个月大的(老年)小鼠中施用Ab68、NMN、ors-Ab68-lpu-NMN的效果。
研究结果表明,衰老组织中的衰老细胞在驱动具有CD38酶活性的免疫细胞积累方面发挥着关键作用,这有助于年龄相关的NAD+水平下降。作者表示,NAD+水平如何随着年龄的增长而下降是复杂的,未来的研究需要检查细胞使用哪些途径来更好地了解衰老中的NAD+生物学。然而,这项研究让我们得以一窥研究人员在弄清细胞NAD+随着年龄的增长而减少背后的细胞机制方面继续取得的进展。
来源:本网编辑 2024.04.20.
参考文献:
Chini CCS et al. CD38 ecto-enzyme in immune cells is induced during aging and regulates NAD+ and NMN levels. Nat Metab. 2020 Nov;2(11):1284-1304.