导言:研究发现,在患有心肌损伤的老年大鼠中,NMN治疗前和褪黑素治疗后具有显著的心脏保护作用。NMN和褪黑素的组合可能是一种很有前途的减轻老年心脏心肌损伤的策略。
心力衰竭的一个主要原因是医学领域中已知的心肌缺血/再灌注(I/R)损伤,即当流向心脏的血液停止(缺血),然后重新启动(再灌注)时发生的心脏损伤。我们现在也知道,衰老会增加我们对心肌缺血的易感性,并限制缺血性损伤后心脏功能的恢复。除此之外,最麻烦的是,衰老的缺血性心脏对常规治疗策略的保护有抵抗力。
Hosseini及其同事发表在《心血管药理学与治疗学杂志》(J Cardiovasc Pharmacol Ther.)上的研究揭示了烟酰胺单核苷酸(NMN)和褪黑素在老年大鼠心肌I/R损伤后的治疗潜力,特别是联合用药时。NMN和褪黑素通过减少损伤大小、改善心肌功能以及其他心脏细胞损伤和功能障碍的措施,对老年大鼠I/R损伤具有保护作用。这表明褪黑素和NMN的组合可以成为一种很有前途的策略来减轻老年心脏的心肌I/R损伤。
治疗因血液流向心脏时停时动造成的损伤
在恢复血流的过程中,心脏会受到炎症以及活性氧(ROS)过量产生、细胞发电结构(线粒体)功能障碍和心脏细胞死亡的影响。这些影响反映在心脏衰老中,导致线粒体功能失调、活性氧(ROS)过度产生和心脏收缩能力下降。因此,心脏病和衰老的这些方面是治疗的关键靶点。
然而,大多数的临床前研究通常使用年轻的动物模型进行,并且只关注一种治疗方法和所讨论疾病的非常有限的方面。这并不能真正概括患有心肌I/R损伤的人类患者,他们通常年龄较大,并表现出其他合并症或心脏病风险因素。因此,通过使用年轻动物模型的实验管道进行的心脏保护治疗并不能很好地转化为人类,通常无法在心肌I/R损伤的临床环境中减少梗死面积并改善患者的预后。克服单独治疗失败并实现最佳心脏保护的一种策略是联合治疗。
褪黑素和NMN能保护心脏吗?
褪黑素(通常用于改善睡眠)因其抗氧化能力和抗炎特性而被公认。褪黑素已被证明对幼年动物具有心脏保护作用,并对线粒体活性产生积极影响。衰老过程中心血管疾病负担的增加与褪黑激素水平低有关。然而,在I/R损伤后,增加血液中褪黑素水平是否能调节ROS的产生或恢复老年心脏组织的心脏细胞功能仍不得而知。
烟酰胺腺嘌呤二核苷酸(NAD+)是许多细胞代谢过程的重要辅因子,在能量产生中起主导作用。但随着年龄的增长和心脏损伤,NAD+水平下降,同时线粒体能量产生减少。烟酰胺单核苷酸(NMN)是NAD+的主要前体,其恢复NAD+细胞含量可以改善与年龄相关的生理功能障碍和各种疾病。
NMN和褪黑素组合可保护心脏
在这项研究中,Hosseini及其同事研究了NMN和褪黑素对老年雄性大鼠I/R损伤的心脏保护和线粒体功能的联合作用。在老龄大鼠I/R损伤前28天,他们每隔一天注射一次NMN(100mg/kg/d)后,再添加褪黑素。然后,他们将心脏与这些大鼠分离,并在造成I/R损伤后,向心脏泵送的液体中添加褪黑素。
他们发现,与单独使用这些化合物相比,NMN和褪黑素的联合治疗对衰老大鼠心脏的保护作用更大。例如,尽管NMN和褪黑素单独使用可以提高这些心脏的泵血能力并减少损伤,但Hosseini及其同事观察到,两者的结合产生的效果更接近于未受伤心脏的水平。
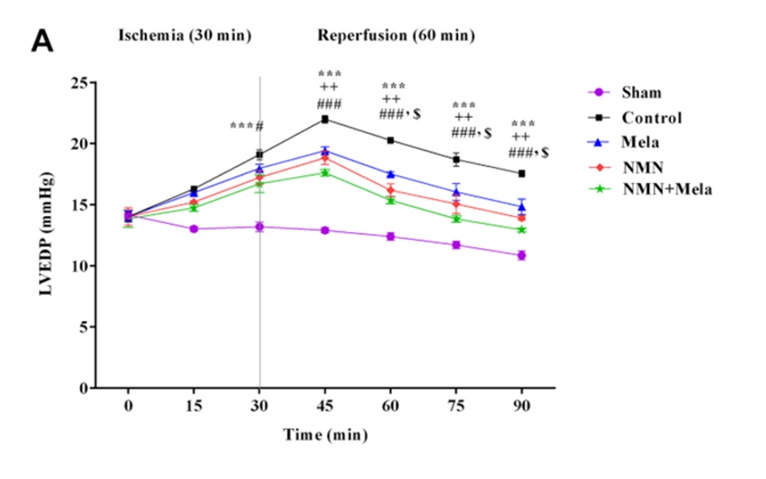
图示. NMN和褪黑素的组合保护心脏功能免受缺血再灌注损伤。在接受30分钟缺血和60分钟再灌注的老年心脏中,当心肌放松时,左心室舒张末压(LVEDP)与NMN和褪黑素(NMN+Mela)联合治疗的未损伤心脏(Sham)最相似。
类似地,乳酸脱氢酶(LDH)水平是I/R损伤期间心脏细胞损伤增加的指标,NMN和褪黑素的联合治疗比这些化合物本身对其影响更大。I/R损伤后心脏的氧化状态也是如此,因为与单独使用这些治疗相比,NMN和褪黑素的联合治疗对线粒体ROS和氧化应激的减少有更大的影响。
关于NAD+水平,I/R损伤后NAD+/NADH水平下降到约为未受伤心脏水平的一半。但是,在缺血前单独或与褪黑素联合施用NMN可以防止缺血诱导的心脏NAD+/NADH比率的降低。Hosseini及其同事提出,这表明NMN进入心脏并提高细胞NAD+水平。褪黑素本身对NAD+/NADH比率的影响很小,尽管是积极的,这并不奇怪,因为它不是NAD+的前体。
这些结果表明,NMN和褪黑素在老年大鼠心脏中的组合可能有助于减轻心肌I/R损伤和增强衰老过程中的心脏保护。然而,进一步的研究对于阐明有助于心脏保护的多种机制中的每一种的作用至关重要。更重要的是,这些数据并没有提供任何关于这种联合治疗的效果是否会转化为人类的见解。
来源:本网编辑 2024.04.12.
参考文献:
Hosseini L et al. Melatonin and Nicotinamide
Mononucleotide Attenuate Myocardial Ischemia/Reperfusion Injury via Modulation
of Mitochondrial Function and Hemodynamic Parameters in Aged Rats. J Cardiovasc
Pharmacol Ther. 2020 May;25(3):240-250.