导言:DNA损伤导致RNA转录停滞。在《自然-遗传学》(Nat Genet)杂志上,研究人员描述了RNA转录缺陷如何构成以前未发现的衰老机制。
图源:互联网
当基因蓝图变得难以阅读时
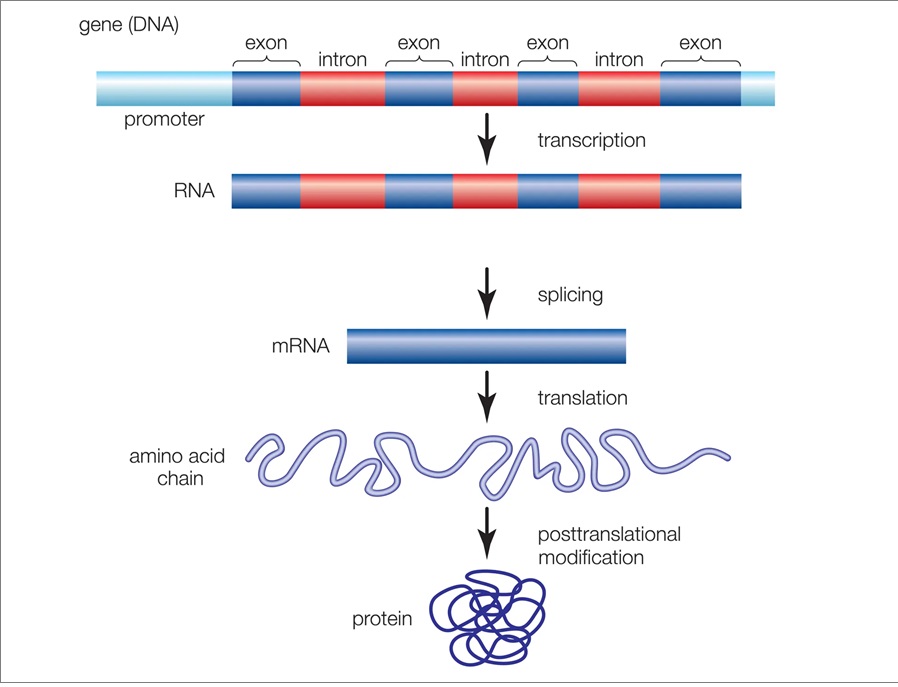
当细胞从DNA蛋白质编码中转录RNA时,基因表达开始。这个过程和几乎所有其他过程一样,都会受到衰老的影响。当然,这背后的一个关键原因是表观遗传改变的标志,即细胞的DNA以有害的方式逐渐甲基化,导致不需要的序列转录,并阻止所需序列的转录。被称为mRNA的小的非编码RNA片段也有助于这种表达变化1。
然而,一项转录组学分析发现,这种先前发现的机制并不完全是错误的;器官中的基因表达往往以同样的方式恶化,这背后一定有另一个原因2。先前对遗传损伤的研究发现,化学诱导的损伤与这种与年龄相关的转录变化有相似之处,遗传损伤本身就是衰老的标志。转录阻断病变出现在DNA上,导致RNA在过程中停滞,并调用修复机制3。先前的一些研究发现,这些病变在正常衰老过程时出现4,但它们对转录造成的损害程度以前从未描述过。
因此,这些研究人员试图首先通过使用自然衰老的小鼠来缩小这一知识差距。
转录能力下降
研究人员将15周大的小鼠与2岁大的小鼠进行了比较;到了那个年龄,小鼠的生命就快结束了。他们给小鼠注射了一种只与新产生的RNA结合的荧光化学物质,发现老年小鼠的新转录显著减少。
仔细观察,研究人员分析了这些新RNA链使用的特定转录化合物。他们发现,使用RNA聚合酶II(RNAPII)的转录显著下降,尽管衰老的肝脏比年轻的肝脏含有更多的这种聚合酶。另一方面,线粒体RNA、RNAPI和RNAPIII转录似乎在很大程度上不受影响;研究人员后来指出,这些化合物与相当短的序列有关。
仔细观察RNAPII是如何被使用和合成的,证实了研究人员的假设。较老的细胞自然地需要与较年轻的细胞相同数量的基于RNAII的转录。底层根本无法实现同样的效果。
挑出原因
通过使用抗体,研究人员发现RNAII的转录在较老和年轻的细胞中以相同的速率开始。转录的开始,第一个千碱基,在两者之间是相同的。研究人员证实了他们之前的结果,发现这些序列在年轻细胞和老年细胞之间的促进作用是相同的。
然后,他们仔细观察了基因表达的变化。他们首先发现,他们独立发现的结果与之前发表的关于转录随年龄变化的研究结果相同。他们还发现,随着基因长度的增加,它们的RNAPII位点越多,在老年动物中成功转录的可能性就越小。转录开始得很好;它只是无法完成。
研究人员回到了他们最初的假设,即DNA损伤是这种转录损失的原因。利用特别容易受到基因损伤的小鼠细胞,他们发现基因损伤的程度与较长RNA序列无法转录之间存在直接关系。用紫外线辐射或氧化应激损伤细胞产生了相同的结果。
强大的下游效应
发现与已知衰老特征相关的多个基因受到转录应激增加的影响。mTOR、胰岛素和生长激素信号传导都受到影响,自噬、蛋白稳态、免疫系统功能和代谢也受到影响。至关重要的是,一种与氧化应激相关的途径受到了影响,这表明这种转录失调可能正在自我放大。
对其他基因转录库的分析,包括果蝇和人类的数据,证实了这种现象发生在动物界和多个组织中。研究发现,分裂不多的细胞比经常分裂的增殖细胞更脆弱,这表明复制可以改善导致RNAPII停滞的DNA损伤。
这是一项初步研究,已经指出了问题的原因,关于任何潜在解决方案的工作尚未发表。目前尚不清楚是否有任何治疗可以减少转录阻断DNA损伤的数量,从而减缓或逆转衰老的一个非常基本的部分。
来源:本网编辑 2024.03.28.
主要参考文献:
Gyenis A et al. Genome-wide RNA polymerase stalling shapes the transcriptome during aging. Nat Genet. 2023 Feb;55(2):268-279.
其他参考文献:
1. Harries LW. MicroRNAs as mediators of
the ageing process. Genes (Basel). 2014 Aug 20;5(3):656-70.
2. Schaum N et al. Ageing hallmarks exhibit
organ-specific temporal signatures. Nature. 2020 Jul;583(7817):596-602.
3. Lans H et al. The DNA damage response to
transcription stress. Nature reviews, Molecular cell biology. 2019
Dec;20(12):766-784.
4. Wang J et al. The oxidative DNA lesions 8, 5′‐cyclopurines accumulate with aging in a tissue‐specific manner. Aging cell. 2012 Aug;11(4):714-6.