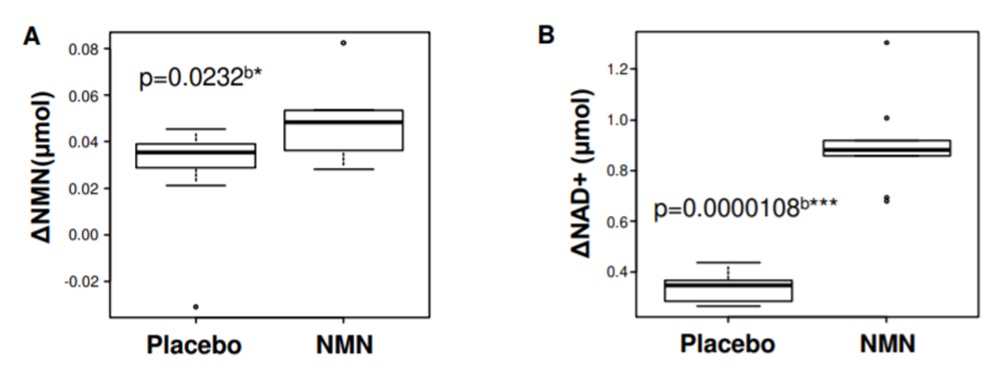
导言:NMN和肠道菌发酵乳杆菌可以消除自由基损伤;NMN和肠道益生菌的组合协同保护小鼠皮肤免受有害的紫外线辐射,促进健康的肌肤老化。
皮肤是人体中最复杂的器官之一,与肠道有着不可分割的联系。皮肤抗衰老已经成为许多学者和临床医生的研究热点,并引起了许多美容爱好者的关注。那么,能否利用已知的这种联系来改善皮肤护理呢?
来自中国重庆大学的Zhao及其同事在《药理学前沿》(Front Pharmacol)2021上发表的一项研究发现,肠道细菌与烟酰胺单核苷酸(NMN)的结合协同改善了紫外线(UV)照射引起的小鼠皮肤损伤。他们发现,小鼠在饮用含有NMN(300mg/kg)和发酵乳杆菌提取物的水时,比单独饮用NMN或细菌有更大的保护作用。这些发现表明,NMN和益生菌通过不同的途径提供皮肤保护,将它们联合使用可能会提供一种增强皮肤健康的手段。
NMN和发酵乳杆菌的抗老化性能
光老化是由于反复暴露于紫外线辐射引起的皮肤过早老化,紫外线辐射主要来自太阳,也来自人造紫外线源。紫外线辐射介导的皮肤光老化的发生和发展涉及多种途径,包括炎症和对氧化应激的反应。研究表明,肠道细菌组成可以调节皮肤炎症,皮肤紫外线辐射会改变肠道细菌组成。弄清楚如何利用皮肤与肠道的联系,可以增强我们保护皮肤免受太阳有害紫外线照射的方式。
发酵乳杆菌已被证明可以平衡肠道细菌(微生物组)的组成。这种肠道细菌还可以增强免疫系统,降低胆固醇水平,减少导致氧化应激的有害分子自由基的存在。这种肠道细菌的潜在抗衰老特性及其清除自由基的能力引起了研究人员的注意,他们正在寻找增强皮肤保护和健康的方法。
另一种抗氧化和抗炎化合物是NMN,它能提高烟酰胺腺嘌呤二核苷酸(NAD+)关键分子的水平,用于产生能量和维持细胞健康。有令人信服的证据表明,服用NMN可以减少肝脏等器官的自由基和炎症,还可以延缓衰老。
一些报道表明NMN和发酵乳杆菌对紫外线损伤的皮肤都有保护作用。出于这些原因,Zhao和同事决定测试NMN和发酵乳杆菌对紫外线辐射损伤皮肤的保护作用。
NMN和发酵乳杆菌协同促进自由基清除
为了测试它们的抗氧化能力,Zhao和同事将NMN和试管中肠道细菌的含量与自由基混合,并测量它们吸收自由基的能力,也就是清除自由基功能。结果发现,将NMN和肠道细菌混合在一起比单独使用NMN或细菌更好地吸收自由基。这种组合也优于维生素C,众所周知,维生素C是一种出色的自由基清除剂。由于皮肤细胞中的自由基在紫外线辐射诱导的衰老中起着关键作用,NMN和细菌对自由基的清除可能说明补充剂的组合如何保护皮肤免受有害的紫外线辐射。
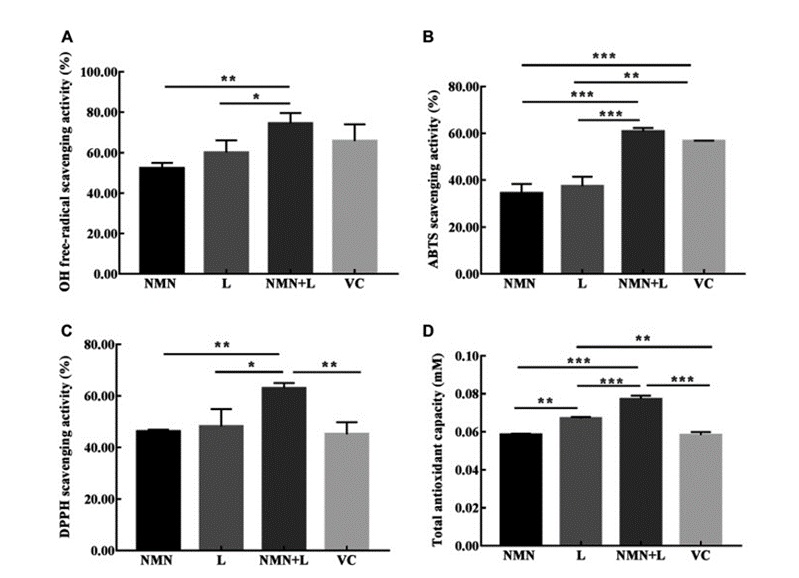
图示. NMN和发酵乳杆菌协同增强自由基清除。图(A)、(B)和(C)描述了3种不同的自由基——OH、ABTS和DPPH—被NMN、发酵乳杆菌(L)、NMN加发酵乳杆菌的吸收情况(NMN+L)和维生素C(VC)。由于维生素C以清除自由基而闻名,研究人员将其自由基吸收(清除)能力与其他治疗方法进行了比较。有趣的是,NMN加发酵乳杆菌处理对三种自由基中的每一种都提供了更好的吸收,这表明它具有有效的清除作用。右下图(D)显示了每种处理吸收的自由基总浓度(抗氧化能力),其中NMN加发酵乳杆菌处理吸收最多。
两种物质结合显著增强皮肤保护
Zhao和同事们随后将他们的实验从试管转移到活体动物身上。他们想弄清楚这种补充剂组合的减少自由基的特性是否能在强烈的两周UVB辐射暴露后保持小鼠皮肤组织的完整性。尽管NMN和发酵乳杆菌本身有明显的影响,但研究小组发现,用这两种物质联合治疗的小鼠显示出与未暴露于UVB辐射的小鼠相似的皮肤组织保存。通过在显微镜下观察皮肤,观察到这种治疗组合显著地保留了皮肤的真皮层(表面下的一层含血管层),类似于未暴露于UVB辐射的小鼠。
此外,暴露于UVB辐射后,真皮层中肥大细胞(指示炎症的细胞)的数量增加了4倍。补充NMN和发酵乳杆菌显著减少了肥大细胞的数量,使得它们在强烈的UVB辐射暴露后仅增加约2倍。因此,联合治疗比NMN或单独的细菌提供了更好的组织保存,表明具有协同保护作用。
结语
先前的研究表明,NMN通过激活维持细胞健康和促进自由基清除的酶,如Sirtuins,增强NAD+的生物合成,以改善小鼠的疾病。然而,对发酵乳杆菌的保护作用的理解仍然难以捉摸,Zhao及其同事表示,这可能与其短链脂肪酸等代谢产物的抗炎作用有关。研究团队补充说,仍然非常需要更好地理解这种细菌的有益作用,尤其是当它与NMN结合时。此外,我们需要进行人体研究,以证明这些物质的组合有多有效。
来源:本网编辑 2024.04.18.
参考文献:
Zhou
X et al. Nicotinamide Mononucleotide Combined With Lactobacillus fermentum
TKSN041 Reduces the Photoaging Damage in Murine Skin by Activating AMPK
Signaling Pathway. Front Pharmacol. 2021 Mar 25;12:643089.