导言:尽管只有很少的人体临床试验,但有证据表明,NAD+前体对人们来说是安全的,其剂量可能会转化为在动物研究上呈现的有益作用。
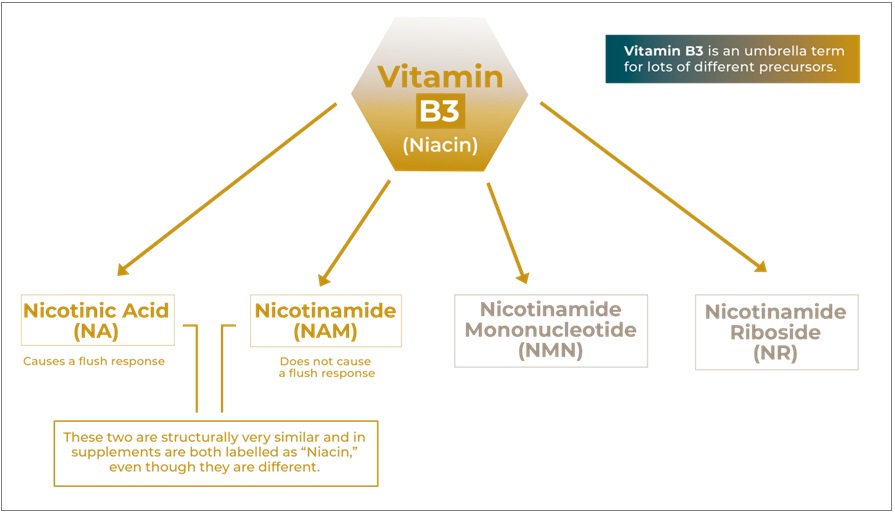
图示,维生素B3及其衍生物(图源:互联网)
烟酰胺腺嘌呤二核苷酸(NAD+)是酶参与大量生化反应所必需的一种化合物,已被发现是激活驱动数百种不同生物过程的酶的关键。在哺乳动物细胞中,NAD+是最丰富的分子之一。鉴于NAD+的活力,人们对提高主要由化学前体组成的NAD+水平的方法越来越感兴趣。然而,对这些NAD+增强剂中有多少可以产生NAD+并发挥有益(或有害)作用了解多少?
NAD+前体具有不同的增强效率、毒性和给药范围
1.烟酰胺(NAM)
NAM是最早用于提高NAD+水平的代谢化合物之一。由于NAM很容易获得(一种维生素B3),并且可以通过细胞膜进入细胞,因此这种前体是用于治疗脑组织NAD+缺乏症的最合理的候选者1。NAM通过细胞膜的能力解释了其对血脑屏障(BBB)的快速渗透,BBB是化合物试图从循环进入神经系统的障碍。但这也表明,NAM可以很容易地通过血流从组织中去除。
然而,众所周知,作为NAD+消耗的副产物,NAM也是依赖NAD+的酶的天然反馈抑制剂。例如,依赖NAD+的酶随着NAM浓度的增加而被抑制,这被认为是NAM在人类中的抗糖尿病作用的驱动因素。
许多研究表明,即使在长期给药期间,也能耐受NAM2-5。这些研究确保了目前广泛采用的每天500-1500mg的长期膳食摄入的安全性。据报道,剂量超过3000mg的人体副作用仅限于几个器官,即肝脏、肾脏、血浆细胞和胰腺β细胞。
2.烟酰胺单核苷酸(NMN)
由于NMN是NAD+的直接前体,理论上它可以绕过限速步骤,更有效地促进NAD+的合成;NMN将直接进入一步酶促生成NAD+6-8。有几份报告显示,腹腔给予NMN可以在注射后15分钟内显著增加脑组织NAD+水平9。这一点,随着NMN特异性转运蛋白的鉴定,支持了NMN主动转运到细胞中转化为NAD+的概念10。
在人类中,一项临床试验研究显示,在10名健康男性中单次服用NMN是安全的,并证实了它可以安全地服用,并且在体内有效代谢11。尽管没有太多的人体研究,但用于研究人体NMN的剂量范围为100-1200mg12,13。目前尚无NMN对体温、血压、脑血流量或其他形式的毒性等生理参数产生显著不良影响的报告。
3.烟酰胺核糖(NR)
提高NAD+水平的另一种选择是补充烟酰胺核糖(NR)14。但是NR在血液中非常不稳定,这使得测量和检测变得困难。由于其不稳定性,通常用于产生有益效果的剂量往往很高。
NR还经过了六项临床试验的测试,其中NR被确定为短期(8天)和长期(6周)使用的安全性,以及经证实的口服有效性15-18。此外,一项为期8周的随机安慰剂对照试验,使用三种不同剂量(最高1000mg)的NR,在超重和健康成年人中进行了测试,报告称NR氯化物是安全的,可以口服。在几项研究中已经观察到血液样本中NR的不稳定性。
临床试验中NMN和NR的口服给药剂量和持续时间
化合物名称 | 剂量 (mg/day) | 持续时间 | 参考来源 |
NMN | 600, 1200 | 6 weeks | Liao et al. 202112 |
NMN | 250 | 10 weeks | Yoshino et al. 202113 |
NR | 250, 500 | 8 weeks | Dellinger et al. 201716 |
NR | 500 | 6 weeks | Martens et al. 201817 |
NR | 1000 | 3 weeks | Elhassan et al. 201918 |
4.烟酸或尼克酸(NA)
烟酸是维生素B3常见的一种,作用包括将食物转化为能量,有助于保持神经系统、消化系统和皮肤健康。烟酸(维生素B3)通常是组成日常多种复合维生素的一部分,但大多数人从他们吃的食物中获得足够的烟酸。研究表明,烟酸可在10个月内提高参与者的NAD+水平,每天750-1000mg19。据报道,每天服用2000至6000mg烟酸会产生严重副作用。
NA代表烟酸的酸形式20,21。临床上常用于治疗高脂血症。据报道,每天摄入1000至3000mg可降低血液甘油三酯水平和低密度脂蛋白(LDL),同时提高高密度脂蛋白(HDL)水平,从而有利于调节LDL:HDL比率。
然而,NA疗法在大多数人中可引起显著的皮肤潮红,从而限制了其临床应用。据报道,口服50mg NA的患者出现轻度皮肤潮红,美国和加拿大的成人NA的耐受上限已设定为每天35mg。NA在高水平的半衰期为1小时时优先从循环中清除,而烟酰胺(NAM)的半衰期为4小时。
需要创建成功提升NAD+的策略
据推测,对长期补充NAD+前体的药理学反应可能会随着时间的推移而改变。这也提出了一个重要的问题,即较高的NAD+水平是否有可能对细胞功能产生有害影响,从而刺激适应性反应。然而,每个人服用NAD+增强剂的策略将根据所寻求的结果而改变,因为这些前体对细胞的影响不同。
来源:本网编辑 2024.04.09.
参考文献:
1. Hwang ES et al. Possible Adverse Effects of High-Dose Nicotinamide: Mechanisms and Safety Assessment. Biomolecules. 2020 Apr 29;10(5):687.
2. Gale EAM et al. European Nicotinamide Diabetes Intervention Trial (ENDIT): a randomised controlled trial of intervention before the onset of type 1 diabetes. Lancet. 2004 Mar 20;363(9413):925-31.
3. Takahashi Y et al. Nicotinamide suppresses hyperphosphatemia in hemodialysis patients. Kidney Int. 2004 Mar;65(3):1099-104.
4. Libri V et al. Epigenetic and neurological effects and safety of high-dose nicotinamide in patients with Friedreich’s ataxia: an exploratory, open-label, dose-escalation study. Lancet. 2014 Aug 9;384(9942):504-13. 5. Phelan MJ et al. Phase II clinical trial of nicotinamide for the treatment of mild to moderate Alzheimer’s disease. J Geriatr Med Gerontol. 2017;3:021.
6. Poddar SK et al Nicotinamide Mononucleotide: Exploration of Diverse Therapeutic Applications of a Potential Molecule. Biomolecules. 2019 Jan 21;9(1):34.
7. Hong W et al. Nicotinamide Mononucleotide: A Promising Molecule for Therapy of Diverse Diseases by Targeting NAD+ Metabolism. Front Cell Dev Biol. 2020 Apr 28;8:246.
8. Khaidizar FD et al. Nicotinamide Phosphoribosyltransferase as a Key Molecule of the Aging/Senescence Process. Int J Mol Sci. 2021 Apr 2;22(7):3709.
9. Klimova N et al. Multi-targeted Effect of Nicotinamide Mononucleotide on Brain Bioenergetic Metabolism. Neurochem Res. 2019 Oct;44(10):2280-2287.
10. Wu LE et al. The elusive NMN transporter is found. Nat Metab. 2019 Jan;1(1):8-9.
11. Irie J et al. Effect of oral administration of nicotinamide mononucleotide on clinical parameters and nicotinamide metabolite levels in healthy Japanese men. Endocr J. 2020 Feb 28;67(2):153-160.
12. Liao B et al. Nicotinamide mononucleotide supplementation enhances aerobic capacity in amateur runners: a randomized, double-blind study. J Int Soc Sports Nutr. 2021 Jul 8;18(1):54.
13. Yoshino M et al. Nicotinamide mononucleotide increases muscle insulin sensitivity in prediabetic women. Science. 2021 Jun 11;372(6547):1224-1229.
14. Mehmel M et al. Nicotinamide Riboside-The Current State of Research and Therapeutic Uses. Nutrients. 2020 May 31;12(6):1616.
15. Trammell SA et al. Nicotinamide riboside is uniquely and orally bioavailable in mice and humans. Nat Commun. 2016 Oct 10;7:12948.
16. Dellinger RW et al. Repeat dose NRPT (nicotinamide riboside and pterostilbene) increases NAD+ levels in humans safely and sustainably: a randomized, double-blind, placebo-controlled study. NPJ Aging Mech Dis. 2017 Nov 24;3:17.
17. Martens CR et al. Chronic nicotinamide riboside supplementation is well-tolerated and elevates NAD+ in healthy middle-aged and older adults. Nat Commun. 2018 Mar 29;9(1):1286.
18. Elhassan YS et al. Nicotinamide Riboside Augments the Aged Human Skeletal Muscle NAD+ Metabolome and Induces Transcriptomic and Anti-inflammatory Signatures. Cell Rep. 2019 Aug 13;28(7):1717-1728.e6.
19. Pirinen E et al. Niacin Cures Systemic NAD+ Deficiency and Improves Muscle Performance in Adult-Onset Mitochondrial Myopathy. Cell Metab. 2020 Jun 2;31(6):1078-1090.e5.
20. Ban TA. Nicotinic acid in the treatment of schizophrenias. Practical and theoretical considerations. Neuropsychobiology. 1975;1(3):133-45.
21. Hageman GJ et al. Nicotinic acid supplementation: effects on niacin status, cytogenetic damage, and poly(ADP-ribosylation) in lymphocytes of smokers. Nutr Cancer. 1998;32(2):113-20.

