衰老细胞在体内积累不仅导致各种慢性疾病,也加速人体老化。Senolytics可选择性地消除衰老细胞,临床前实验和人体研究显示其为人类健康和长寿带来深远影响。
目录
1. Senolytics释义
10.参考文献
随着年龄的增长,在我们的身体中,衰老、非增殖性的衰老细胞的数量会增加,这些细胞会向周围细胞释放炎症分子1。衰老细胞释放的分子组合(衰老相关分泌表型[SASP])也诱导与之接触的健康细胞衰老2。尽管大多数细胞都达到了程序性细胞死亡(凋亡)的临界点,但随着年龄的增长,越来越多的细胞变得衰老,并在分子凋亡的提示下存活下来。由于我们的免疫力会随着年龄的增长而减弱,我们的免疫系统也很难处理衰老的细胞3。
这种与年龄相关的衰老细胞积累促进了组织炎症和器官损伤,导致器官功能障碍和疾病。因此,一些研究人员提出与年龄相关的衰老细胞积累是人体衰老的原因之一4。
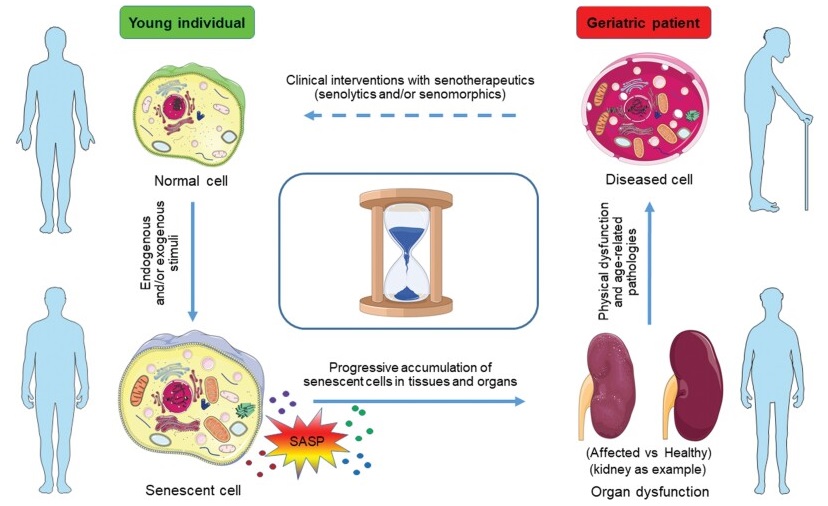
图1. 衰老细胞对衰老和相关疾病有重大影响(Sun et al.,2022|Life Med)
科学家们认为消除衰老细胞是一种对抗衰老不利影响的方法,即减少炎症和改善组织功能5,6。
Senolytics疗法(或称衰老细胞清除术)是指让凋亡通路(SCAP)暂时性失效,从而选择性诱导衰老细胞凋亡的技术,临床已证明可延缓、预防或减轻多种疾病7。为此,研究人员最近开发了一类新的补充剂即Senolytics,其中大部分来自水果和蔬菜中发现的植物多酚。这些新药可以选择性地触发衰老细胞的细胞死亡(凋亡),而不会显著损害健康细胞。
Senolytics通过靶向促生存途径发挥作用,衰老细胞利用这些途径来逃避凋亡。消除衰老细胞的一大挑战是,这些细胞有多种类型,来自不同的组织,它们依赖不同的细胞凋亡逃避途径8。出于这个原因,使用多种Senolytics,每种都靶向不同的途径,可能是终止大量衰老细胞所必需的9。此外,一些衰老细胞在伤口愈合中发挥着重要作用10,因此在决定靶向哪个细胞之前,弄清楚每个衰老细胞群体的作用至关重要。
在过去的十年里,研究人员开始更多地相信,去除衰老细胞可以对抗衰老的一些不利影响。沿着这些思路,许多啮齿动物的研究已经给出了积极的结果,推动了人们对Senolytic疗法的热情。
实例包括使用Senolytic治疗剂槲皮素,当它与化疗药达沙替尼(Dasatinib)组合时,被发现可改善自然衰老和动脉粥样硬化小鼠模型的心脏功能11。另一项使用达沙替尼和槲皮素的研究发现,这种Senolytic疗法组合增强了辐射损伤的小鼠的运动能力12。达沙替尼和槲皮素的Senolytic组合也延缓了早衰小鼠身体功能障碍的发生13。这些研究是使用Senolytic治疗剂达沙替尼和槲皮素的动物研究的一些主要发现之一。
漆黄素(Fisetin)是一种在草莓和洋葱等食物中发现的植物类黄酮,在小鼠研究中获得了积极的发现。Fisetin可减轻与年龄相关的疾病,并使健康小鼠的平均寿命延长约20%14。问题仍然是,在啮齿类动物研究中,达沙替尼和槲皮素以及Fisetin的发现将在多大程度上转化为人类效应。如图2所示,注射Fisetin饮食可使小鼠的平均寿命延长约25%,包括Fisetin(橙色线)在内的饮食可以提高存活率,因此与正常饮食(黑色线)的小鼠相比,中位寿命(星号)延长约25%。
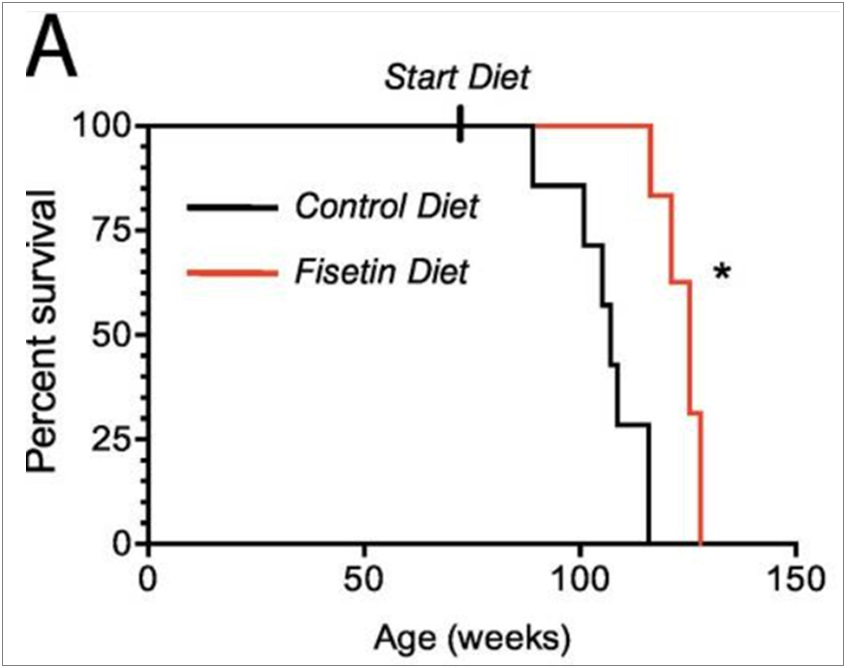
图2. 注射Fisetin饮食可使小鼠的平均寿命延长约25%(Yousefzadeh,2018|EBioMedicine)
另一种很有前景的Senolytic治疗剂为原花青素C1(PCC1),它是一种在葡萄、未成熟苹果和肉桂中发现的植物衍生分子。有趣的是,一项研究表明,给24个月大的衰老小鼠补充PCC1可使其剩余寿命延长近64%15。PCC1还没有像Fisetin和槲皮素那样引起人们的关注,因此未来的研究应该调查该分子的长寿潜力。
早期人体试验的数据表明,Senolytics能有效地消除衰老细胞,缓解炎症,减轻人体虚弱。阿尔茨海默病、新冠肺炎、糖尿病、眼部疾病、肺纤维化、骨关节炎、骨质疏松症、骨髓移植和儿童癌症幸存者的临床试验目前正在进行中。在这些研究得出结论之前,现在说Senolytics对老年人的有效性还为时尚早。
由美国最著名医院Mayo Clinic(梅奥诊所)开展的第一项Senolytic临床试验证明,服用达沙替尼和槲皮素的肺瘢痕(特发性肺纤维化)患者的身体功能有所改善16。另一项人体试验报道,达沙替尼和槲皮素治疗可减少糖尿病肾病患者脂肪组织中的衰老细胞负担17。此外,在这些患者中,引起炎症的循环SASP因子减少。
最近,一项达沙替尼和槲皮素治疗阿尔茨海默病的I期临床试验报告称,间歇性Senolytic给药可降低阿尔茨海默病病理学的一个标志—tau蛋白聚集体。同一项研究表明,达沙替尼和槲皮素可以减少神经炎症,保护神经元,并部分恢复大脑的血液流动18。
鉴于与Senolytics相关的有希望的发现及其可靠的安全性,已经启动了一系列研究其临床潜力的新试验。此类达沙替尼和槲皮素的研究包括轻度认知障碍和阿尔茨海默病、肝病和癌症的研究19,20。Fisetin也在用于研究乳腺癌21、Covid-1922和腕管综合征23等疾病。如果这些试验产生了积极的结果,那么使用Senolytic药物对抗与年龄相关的生理衰退可能会变得越来越普遍。
研究人员认为,糖尿病是导致过早衰老和心血管疾病和神经退行性疾病等与年龄相关疾病发展的主要因素之一。细胞衰老被认为在胰岛素抵抗和其他糖尿病相关并发症的发展中起着至关重要的作用。此外,当一个人患有糖尿病时,这会导致衰老细胞形成增加。根据这些原理,持续暴露在高血脂和血糖水平下,这两种糖尿病的风险因素都会引发细胞衰老24。一旦衰老细胞形成,它们就会向周围细胞和组织释放SASP因子,引发更多细胞进入敏感状态,并增加患糖尿病的风险。因此,使用Senolytics可能有助于预防糖尿病的发生。
2014年进行的一项小型临床研究显示16,患有特发性肺纤维化肺组织瘢痕形成疾病的患者在接受达沙替尼和槲皮素这两种Senolytics治疗后,身体功能有所改善。这些结果显示了Senolytics改善肺部健康的前景,因为达沙替尼和槲皮素有可能治疗这种肺部疾病。这些结果需要未来使用更大规模的研究以进行确认。
与糖尿病相关的肾病患者在服用Senolytics后,身体功能有所改善。美国最知名医院Mayo Clinic的一项研究表明,达沙替尼和槲皮素治疗可以减少糖尿病肾病患者脂肪组织中的衰老细胞17。此外,在达沙替尼和槲皮素治疗后,使附近细胞和组织发炎的循环SASP因子减少。这些发现使我们离证实啮齿动物研究数据更近了一步,这些数据显示Senolytics缓解与年龄相关的疾病,也适用于人类。
骨关节炎是一种与年龄相关的疾病,患者会失去关节软骨,从而导致身体衰弱,使他们无法正常工作。患有骨关节炎的人抱怨走路时极度疼痛,对行动能力产生不利影响。患有这种疾病的老年人由于疼痛而不多走路,以避免体力消耗和加剧其身体衰弱。有鉴于此,找到有效的方法来治疗这种情况是至关重要的。
最近,研究人员表明,软骨生成细胞(软骨细胞)会衰老,向周围细胞和关节释放SASP因子25。用Senolytics靶向这些细胞可以提供治疗骨关节炎的有效方法。令人鼓舞的是,最近的一项研究表明,Senolytic ABT-263可以促进提取自骨关节炎患者的软骨生成干细胞的功能26。未来的研究需要确定这种用于骨关节炎患者的Senolytic化合物是否能改善他们的身体功能。
阿尔茨海默病(又称老年痴呆)是是一种与年龄有关的疾病,其特征是认知能力逐渐下降,包括大脑中淀粉样蛋白β斑块的积聚。有趣的是,衰老细胞中的蛋白质聚集体包括淀粉样蛋白β斑块27。因此,用Senolytics抑制衰老细胞的积累可能是减轻阿尔茨海默病相关病理的一种方法。
构成大脑血液和大脑之间屏障(血脑屏障)的细胞之一是星形胶质细胞。除了血脑屏障外,星形胶质细胞还具有许多脑保护的作用28。当星形胶质细胞衰老时,它们会向周围的细胞和组织释放大量的SASP因子,限制淀粉样蛋白β斑块的清除。这种情况会导致淀粉样蛋白β斑块水平升高,并促进阿尔茨海默病症状的恶化29。
在一项小型临床试验中发现,达沙替尼和槲皮素的Senolytic组合可以减轻SASP因子的积累,减缓衰老向周围细胞的扩散18。因此,达沙替尼和槲皮素可以通过抑制SASP因子的传播来缓解阿尔茨海默病,但需要更多的临床试验来加以证实。
癌症始于单个细胞,它获得了一个基因突变,增加了分裂的能力。有了这些癌症突变,细胞可以无限期地分裂和增殖。癌细胞还与附近的其他健康细胞竞争营养。因此,癌细胞在营养获取方面胜过健康细胞,导致其数量超过健康细胞,癌症得以快速生长。
当癌症细胞衰老时,其分裂和增殖能力下降。因此,当衰老时,它们的增殖和迁移到身体其他部位的能力就会减弱30。此外,癌细胞释放的SASP因子对其附近的其他癌细胞具有抗癌作用。出于这些原因,一些研究人员认为,诱导癌症细胞衰老可以阻止其生长和扩散31-33。
帕博西尼(Palbocilib)是一种很有前途的诱导癌细胞衰老的Senolytics,它选择性地抑制促进癌细胞增殖的蛋白质34。此外,这些蛋白质的抑制导致癌症细胞生长停滞和衰老。Palbocilib在乳腺癌、黑色素瘤、胃癌、肝细胞癌和脂肪肉瘤方面显示出有前景的发现34-38。
虽然随着年龄的增长,衰老细胞在体内积累的影响正在研究中,但是已有证据表明这种积累在衰老中起着关键作用,这使其成为抗衰老药物的一个很有前途的靶点。因此,Senolytics为选择性消除衰老细胞以减少炎症和改善组织健康提供了一种潜在的新选择。
来源:本网编辑2024.04.25.首版
1. Song S et al. Senescent Cells: Emerging
Targets for Human Aging and Age-Related Diseases. Trends Biochem Sci. 2020 Jul;
45(7): 578–592.
2. Borodkina AV et al. "Social
Life" of Senescent Cells: What Is SASP and Why Study It? Acta Naturae.
2018 Jan-Mar;10(1):4-14.
3. Lee K-A et al. Immune Senescence,
Immunosenescence and Aging. Front Aging. 2022; 3: 900028.
4. van Deursen JM. The role of senescent
cells in ageing. Nature. 2014 May 22;509(7501):439-46.
5. von Kobbecorresponding C. Targeting
senescent cells: approaches, opportunities, challenges. Aging (Albany NY). 2019
Dec 31; 11(24): 12844–12861.
6. Qiu Z et al. Targeting senescent cell
clearance: An approach to delay aging and age-associated disorders.
Translational Medicine of Aging.
2021;v.5;p.1-9
7. Chaib S et al. Cellular senescence and
senolytics: the path to the clinic. Nat Med. 2022 Aug;28(8):1556-1568.
8. Hu L et al. Why Senescent Cells Are
Resistant to Apoptosis: An Insight for Senolytic Development. Front Cell Dev
Biol. 2022 Feb 16:10:822816.
9. Gasek NS et al. Strategies for Targeting
Senescent Cells in Human Disease. Nat Aging. 2021 Oct;1(10):870-879.
10. Andrade AM et al. Role of Senescent
Cells in Cutaneous Wound Healing. Biology (Basel). 2022 Dec; 11(12): 1731.
11. Roos CM et al. Chronic senolytic
treatment alleviates established vasomotor dysfunction in aged or
atherosclerotic mice. Aging Cell. 2016 Oct;15(5):973-7.
12. Zhu Y et al. Identification of a novel
senolytic agent, navitoclax, targeting the Bcl-2 family of anti-apoptotic
factors. Aging Cell. 2016 Jun;15(3):428-35.
13. Fuhrmann-Stroissnigg H et al.
Identification of HSP90 inhibitors as a novel class of senolytics. Nat Commun.
2017 Sep 4;8(1):422
14. Yousefzadeh MJ et al. Fisetin is a
senotherapeutic that extends health and lifespan. EBioMedicine. 2018
Oct:36:18-28.
15. Xu Q et al. The flavonoid procyanidin
C1 has senotherapeutic activity and increases lifespan in mice. Nat Metab. 2021
Dec;3(12):1706-1726.
16. Justice JN et al. Senolytics in
idiopathic pulmonary fibrosis: Results from a first-in-human, open-label, pilot
study. EBioMedicine. 2019 Feb:40:554-563.
17. Hickson LJ et al. Senolytics decrease
senescent cells in humans: Preliminary report from a clinical trial of
Dasatinib plus Quercetin in individuals with diabetic kidney disease.
EBioMedicine. 2019 Sep:47:446-456.
18. Gonzales MM et al. Senolytic Therapy to
Modulate the Progression of Alzheimer's Disease (SToMP-AD): A Pilot Clinical
Trial. J Prev Alzheimers Dis. 2022;9(1):22-29.
19. Available at. https://clinicaltrials.gov/study/NCT04785300
20. Available at. https://clinicaltrials.gov/study/NCT05724329
21. Available at. https://clinicaltrials.gov/study/NCT05595499
22. Available at. https://clinicaltrials.gov/study/NCT04476953
23. Available at. https://clinicaltrials.gov/study/NCT05416515
24. Palmer AK et al. Cellular Senescence in
Type 2 Diabetes: A Therapeutic Opportunity. Diabetes. 2015 Jul;64(7):2289-98.
25. Coryell PR et al. Mechanisms and
therapeutic implications of cellular senescence in osteoarthritis. Nat Rev
Rheumatol. 2021 Jan;17(1):47-57.
26. Miura Y et al. Clearance of senescent
cells with ABT-263 improves biological functions of synovial mesenchymal stem
cells from osteoarthritis patients. Stem Cell Res Ther. 2022 Jun 3;13(1):222.
27. Khan AB et al. An Insight into the
Protein Aggregation in Alzheimer's Disease and its Inhibition. Protein Pept
Lett. 2023;30(11):900-912.
28. Abbott NJ et al. Astrocyte–endothelial
interactions at the blood–brain barrier. Nat Rev Neurosci. 2006 Jan;7(1):41-53.
29. Yue Q et al. Emerging roles of
astrocytes in blood-brain barrier disruption upon amyloid-beta insults in
Alzheimer’s disease. Neural Regen Res. 2023 Sep; 18(9): 1890–1902.
30. Niklander SE et al. Senescent Cells in
Cancer: Wanted or Unwanted Citizens. Cells. 2021 Nov 26;10(12):3315.
31. Bousset L et al. Targeting senescence
as an anticancer therapy. Mol Oncol. 2022 Nov; 16(21): 3855–3880.
32. Saretzki G. Cellular senescence in the
development and treatment of cancer. Curr Pharm Des. 2010 Jan;16(1):79-100.
33. Wang L et al. Exploiting senescence for
the treatment of cancer. Nat Rev Cancer. 2022 Jun;22(6):340-355.
34. Cadoo KA et al. Palbociclib: an
evidence-based review of its potential in the treatment of breast cancer.
Breast Cancer (Dove Med Press). 2014; 6: 123–133.
35. Schmidt M et al. Palbociclib-The First
of a New Class of Cell Cycle Inhibitors. Recent Results Cancer Res.
2018:211:153-175.
36. Bi H et al. Palbociclib induces cell
senescence and apoptosis of gastric cancer cells by inhibiting the Notch
pathway. Oncol Lett. 2021 Aug;22(2):603.
37. Bollard J et al. Palbociclib
(PD-0332991), a selective CDK4/6 inhibitor, restricts tumour growth in
preclinical models of hepatocellular carcinoma. Gut. 2017 Jul;66(7):1286-1296.
38. Jost T et al. Palbociclib Induces Senescence
in Melanoma and Breast Cancer Cells and Leads to Additive Growth Arrest in
Combination With Irradiation. Front Oncol. 2021 Oct 13:11:740002.
