导言:华盛顿大学医学院的研究人员在小鼠体内发现了一种名为Slc12a8的NMN特异性转运蛋白。
烟酰胺单核苷酸(NMN)是细胞用来合成必需分子NAD+的前体,被认为可以对抗与组织NAD+水平下降相关的年龄相关疾病和病症1-14。但NMN是如何被细胞吸收的还不完全清楚。
2019年在《自然代谢》(Nat Metab)杂志上发表的一项研究中,华盛顿大学医学院的研究人员鉴定了一种名为Slc12a8的基因,该基因编码一种特定的NMN转运蛋白。在Alessia Grozio博士领导下,研究小组发现Slc12a8在小鼠小肠中大量存在。这种转运蛋白似乎存在于人类、小鼠、斑马鱼、果蝇和蛔虫中。当删除时,NMN不再转运到小鼠细胞中,无论是在培养物中还是在活体动物中。
Grozio及其同事说:“我们的工作确定了第一个NMN转运蛋白,并证明Slc12a8在调节肠道NAD+代谢方面发挥着关键作用。”
身体如何吸收NMN?
NMN已被提议作为年龄相关疾病预防的治疗剂。研究发现,在衰老过程中,许多组织的NAD+水平下降,包括肌肉、肝脏、脂肪组织、大脑、胰腺、脾脏、心脏、肾脏和肺部,这些都会导致与年龄相关的疾病。研究报告称,NMN在改善疾病和对抗与年龄相关的生理下降方面具有积极作用1-14。
NMN被迅速吸收到组织和细胞中,用于合成一种称为烟酰胺腺嘌呤二核苷酸(NAD+)的必需分子。这就是为什么顶尖科学家提出,体内存在一种有效的转运蛋白,可以将NMN直接吸收到组织和器官中。在肠道吸收的NMN在2到3分钟内进入血液循环,并在摄入后的10-30分钟内运输到组织5,7,14。NMN随后立即用于NAD+生物合成,并在摄取后的60分钟内显著增加细胞中的NAD+浓度5。然而,NMN如何转运到细胞和组织中仍不完全清楚。
Slc12a8是NMN运输工具
为了鉴定所提出的NMN转运蛋白,Grozio及其同事分析了包括肝脏、胰腺和大脑在内的多种组织中的基因活性。通过一系列实验来确定参与NMN穿梭进入细胞的分子,Grozio团队发现了一种名为Slc12a8的转运蛋白基因。研究小组在小鼠的小肠和胰腺中发现了高水平的Slc12a8转运蛋白基因活性,在肝脏和脂肪组织中发现了中等水平。
科学家们进行了进一步的实验,以证实Slc12a8基因编码NMN的转运蛋白,而不是另一种NAD+前体。他们这样做的一种方法是阻断另一种NAD+生物合成前体烟酰胺核糖(NR)进入肝细胞,并在补充NMN后寻找NAD+水平的增加。给予NMN和NR摄取抑制剂的细胞在几分钟内NMN显著增加,表明存在这种NMN转运蛋白。重要的是,当它们从基因上降低Slc12a8的水平时,这种NMN对细胞的快速摄入就消失了。
为了进一步证实Slc12a8基因编码NMN转运蛋白,科学家团队将转运蛋白插入称为NIH3T3细胞的细胞中。在正常情况下,这些细胞对NMN的摄取非常弱。通过增加Slc12a8转运蛋白基因,与未修饰的相应细胞相比,NIH3T3细胞在细胞中具有高得多的NMN水平。
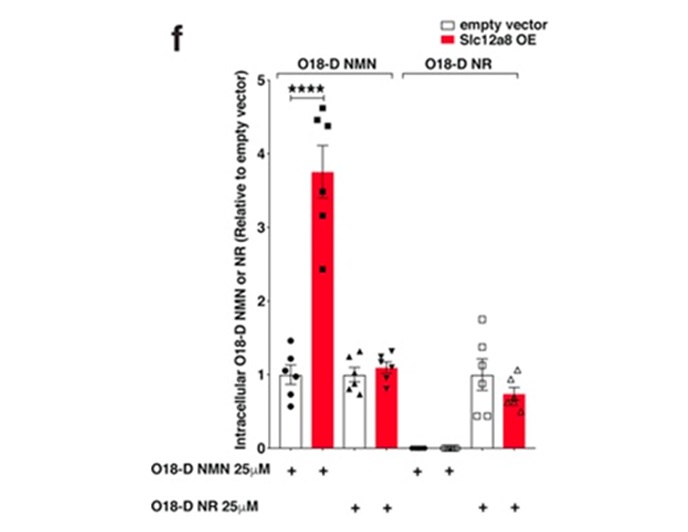
图1.(图源:Grozio et al. 2019)Slc12a8特异性转运NMN,但不转运烟酰胺核糖(NR)。与对照细胞相比,具有增加的Slc12a8水平的细胞(Slc12a8-OE)显示出大约4倍高的O18-D-NMN摄取,但O18-D-NR没有增加,显示出明确的NMN摄取。另一方面,当用25μM O18-D-NR处理时,在Slc12a8 OE和对照细胞(空载体)中都检测到O18-D-NMN合成的等效水平和O18-D-NR-的等效转运。这些结果清楚地表明,Slc12a8以微小的顺序特异性地运输NMN,而不是NR。
Grozio及其同事还研究了Slc12a8是否作为活小鼠NMN细胞摄取的转运蛋白发挥作用。通过降低活小鼠体内Slc12a8的水平,研究人员发现NMN给药后NMN细胞摄入减少。有趣的是,研究小组发现,在老年小鼠中,Slc12a8水平在老年小鼠肠道中增加。他们认为,这试图抵消随着年龄的增长而出现的NAD+水平的下降。
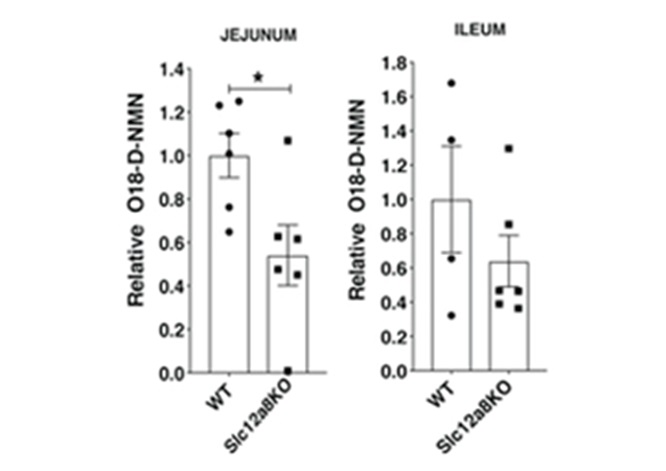
图2.(图源:Grozio et al. 2019)与非转基因小鼠(WT)相比,在小鼠中基因敲低Slc12a8(Slc12a8KO)可降低小肠中NMN的摄取。
Grozio及其同事总结道:“Slc12a8 NMN转运蛋白的鉴定和表征进一步加深了我们对NMN作为关键的系统NAD+中间体的生理重要性的理解。”。“因为NMN在小鼠中表现出显著的减轻年龄相关生理衰退的作用,鉴定可以促进Slc12a8蛋白的NMN转运功能的化合物将为开发更有效的抗衰老干预措施提供一个有趣的机会,并结合NMN给药。
来源:本网编辑 2024.04.15.
主要参考文献:
Grozio A et al. Slc12a8 is a nicotinamide mononucleotide transporter. Nat Metab. 2019 Jan;1(1):47-57.
其他参考文献:
1. Canto C et al. NAD+ Metabolism and the Control of Energy Homeostasis: A Balancing Act between Mitochondria and the Nucleus. Cell Metab, 2015 Jul 7;22(1):31-53.
2. Caton PW et al. Nicotinamide mononucleotide protects against pro-inflammatory cytokine-mediated impairment of mouse islet function. Diabetologia, 2011; 54(12): 3083-3092.
3. de Picciotto NE et al. Nicotinamide mononucleotide supplementation reverses vascular dysfunction and oxidative stress with aging in mice. Aging Cell 2016 Jun;15(3):522-30.
4. Gomes AP et al. Declining NAD+ Induces a Pseudohypoxic State Disrupting Nuclear-Mitochondrial Communication during Aging. 2013 Dec 19;155(7):1624-38.
5. Grozio A et al. Slc12a8 is a nicotinamide mononucleotide transporter. 2019 Jan;1(1):47-57.
6. Long AN et al. Effect of nicotinamide mononucleotide on brain mitochondrial respiratory deficits in Alzheimer’s disease-relevant murine model. BMC Neurology. 2015 Mar 1:15:19.
7. Mills KF et al. Long-term Administration of Nicotinamide Mononucleotide Mitigates Age-Associated Physiological Decline in Mice. Cell Metab. 2016 Dec 13;24(6):795-806.
8. Rajman L et al. Therapeutic Potential of NAD-Boosting Molecules: The In Vivo Evidence. Cell Metab. 2018 Mar 6;27(3):529-547
9. Stein LR et al. Specific ablation of Nampt in adult neural stem cells recapitulates their functional defects during aging. 2014 Jun 17;33(12):1321-40.
10. Verdin E. NAD+ in aging, metabolism, and neurodegeneration. Science. 2015 Dec 4;350(6265):1208-13.
11. Wang X et al. Nicotinamide mononucleotide protects against beta-amyloid oligomer-induced cognitive impairment and neuronal death. Brain Res. 2016 Jul 15:1643:1-9.
12. Yamamoto T et al. Nicotinamide Mononucleotide, an Intermediate of NAD+ Synthesis, Protects the Heart from Ischemia and Reperfusion. PLoS ONE. 2014 Jun 6;9(6):e98972.
13. Yoshino J et al. NAD+ Intermediates: The Biology and Therapeutic Potential of NMN and NR. Cell Metab. 2018 Mar 6;27(3):513-528.
14. Yoshino J et al. Nicotinamide Mononucleotide, a Key NAD+ Intermediate, Treats the Pathophysiology of Diet- and Age-Induced Diabetes in Mice. Cell Metab. 2011 Oct 5;14(4):528-36.

